HOME > 分担研究概要 > 微量放射性薬剤を用いたナノバイオイメージング研究と健康科学への応用
分担研究概要

微量放射性薬剤を用いたナノバイオイメージング研究と健康科学への
応用
田代 学
サイクロトロン・ラジオアイソトープセンター
サイクロトロン核医学研究部 准教授
E-mail:![]()
1. はじめに
放射性薬剤を投与して体内深部の生体反応を体外計測する手法は、1943年にノーベル化学賞を受賞したジョージ・フォン・ヘヴェシー博士が「トレーサー法」として20世紀初期に創始したものである。現在は、コンピューター断層法の技術と融合し、ポジトロン放出断層法(PET)として核医学の分野において確立されている。薬剤を高い比放射能で標識することにより、1〜数ナノモル程度の放射性薬剤を体内に投与するだけで体内の微量物質の動態が観察できるため、まさにナノバイオイメージングに最適なツールといえる。
我々は、放射線技術の医学利用と健康科学への応用を目指しつつ、PET研究を中心とした以下の研究テーマを推進していく計画である。
2. 画像解析と医工学研究開発
2.1 神経伝達機能ナノバイオイメージングにおけるモデル化および簡易定量法の確立
研究テーマの一つとして「ヒトの精神機能の解明」が挙げられる。現代生活におけるストレスは精神神経疾患の増加の一因と考えられており、社会の高齢化とともに認知症や生活習慣病も増加している。こうした問題への対策を検討する上でナノバイオイメージング技術は有効な方法論となりうる。
ヒトの脳内において神経伝達物質はごく微量で強い効果を発現している。一方、物質量自体が少ないため、神経伝達機能を分子レベルでイメージングすることは容易ではないが、PETを用いることで定量化が可能である。その際、血液中および脳組織中の放射性薬剤濃度の時間的変化のデータを用いて、神経伝達機能を定量できる。我々は、これまでヒスタミン、ドーパミン神経系の神経伝達機能を非侵襲的に測定するためのモデル化研究を行い臨床に応用してきた[1,2]。あわせて、薬剤副作用による脳の反応性の変化についても調べている[3]。現在は、アルツハイマー病患者の脳におけるβアミロイドタンパクの蓄積量と定量化するためのモデル構築と画像解析も行っている[4](図1)。そうしたモデル構築研究も進めつつ、MRIとPET画像の重ね合わせの処理速度と精度を向上させるための情報工学的研究も進めている(図1)。
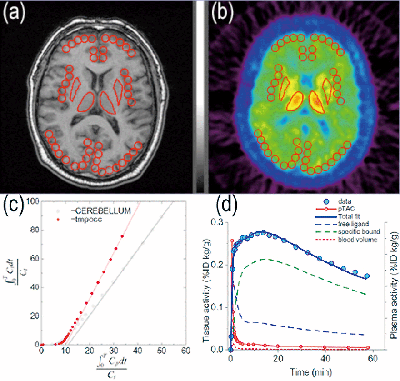
図1. Examples of pharmacokinetic analysis; regions of interest (ROI) defined in co-registered
(a) MRI and (b) PET images, (c) quantification based on graphical analysis and (d) compartment model analysis.
2.2 ナノバイオイメージング技術の予防医学・健康生成科学への応用
世界保健機構(WHO)によれば、「健康」とは「完全な肉体的、精神的及び社会的福祉の状態であり、単に疾病または病弱の存在しないことではない」と定義されている。いわゆる医療におけるQuality of Life (QOL)が重視されることはいうまでもなく、今日では日常生活におけるQOLをも視野にいれた研究が期待される時代に突入している。
一般に、わが国においては、放射線に対する不安感は欧米諸国よりも強いと考えられているが、高感度PETを用いて放射性薬剤の投与量を極限まで抑えることにより、年間自然放射線被曝を大きく下回る被曝量で有用な臨床データを得ることができる。放射線の医学利用において、予防医学・健康生成科学への応用も重要となるだろう。
これまで我々は、PETを用いて、がんに罹患された方(以後、がん患者と表記)の脳代謝が「抑うつ度」を反映して変化していることを報告し、患者の心理評価にPETが利用できる可能性を提案した。そして、心理状態と免疫機能が局所脳活動を介して相互に変化している可能性を初めて指摘し、効果的な治療法の検証にPETが有用である可能性を示した[5](図2)。また、我々はランニング、自転車などの日常的な運動にともなう骨格筋[6]、心筋、脳[7,8]のエネルギー代謝マップを作成した。メタボリック・シンドロームを代表とする生活習慣病に対する効果的な運動療法を検証することも可能である。近年の価値観の多様化により、運動だけでなく代替療法も注目されており、代替療法の効果に関する科学的検証も可能である。
今後は、心理社会的因子と健康の関係を解明するとともに、全身臓器活動のモデル化を行い、全身臓器機能連関マップの構築を目指す。
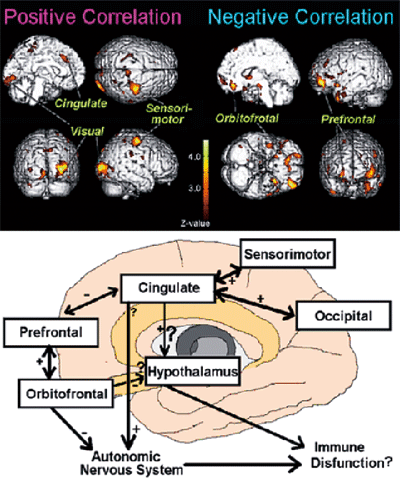
図2. Brain regions of positive and negative correlation to cellular immunity (Natural killer cell activity) in cancer patients (TOP); A hypothesized model of neuro-immune interaction in human (BOTTOM).
2.3 高分解能乳がん診断専用PETカメラの開発
わが国において平成19年より施行された「がん対策基本法」により、がんの診断、治療における質の向上が強く要求される時代になってきた[7]。食生活の欧米化とともに、乳がんの発症率が年々増加しており、より効果的な診断法の確立が期待されている。
我々は、腫瘍空間分解能が約1mmの乳癌診断専用のポジトロンイメージングシステムであるPositron Emission Mammography(PEM)の開発を進めている。近い将来、がん診断におけるナノバイオイメージングにも貢献できるものと期待する。
3. まとめ
このように微量放射性薬剤を用いたナノバイオイメージングには様々な可能性が秘められており、未知の可能性の開拓が進んでいくであろう。しかし、今後のさらなる発展には医学、薬学、工学、情報工学のさらなる絶妙な融合が重要となる。多様な分野の若手研究者がダイナミックに相互作用する人材育成の場が提供できれば幸甚である。
文 献
[1] Tashiro M, Duan X, Kato M, et al. Brain histamine H1 receptor occupancy of orally administered antihistamines, bepotastine and diphenhydramine, measured by PET with [11C]doxepin. Br J Clin Pharmacol 65, 811-821, 2008.
[2] Tashiro M, Mochizuki H, Sakurada Y, et al. Brain histamine H receptor occupancy of orally administered anti-histamines measured by positron emission tomography with [11C]doxepin in a placebo-controlled crossover study design in healthy subjects: a comparison of olopatadine and ketotifen. Br J Clin Pharmacol 61, 16-26, 2006.
[3] Tashiro M, Sakurada Y, Mochizuki H, et al. Effects of a sedative antihistamine, D-chlorpheniramine, on regional cerebral perfusion and performance during simulated car driving. Hum Psychopharmacol 23, 139-150, 2008.
[4] Kudo Y, Okamura N, Furumoto S, Tashiro M, et al. 2-(2-[2-Dimethyl aminothiazol-5-yl]ethenyl)-6-(2[fluoro] ethoxy) benzoxazole: a novel PET agent for in vivo detection of dense amyloid plaques in Alzheimer's disease patients. J Nucl Med 48, 553-561, 2007.
[5] Tashiro M, Itoh M, Kubota K, et al. Relationship between trait anxiety, brain activity and natural killer cell activity in cancer patients: a preliminary PET study. Psychooncology 10, 541-546, 2001.
[6] Fujimoto T, Itoh M, Tashiro M, et al. Glucose uptake by individual skeletal muscles during running using whole-body positron emission tomography. Eur J Appl Physiol 83, 297-302, 2000.
[7] Tashiro M, Itoh M, Fujimoto T, et al. Application of positron emission tomography to neuroimaging in sports sciences. Methods, 2008 (in press).
[8] Tashiro M, Itoh M, Fujimoto T, Fujiwara T, Ota H, Kubota K, Higuchi M, Okamura N, Ishii K, Bereczki D, and Sasaki H. 18F-FDG PET mapping of regional brain activity in runners. J Sports Med Phys Fitness 41, 11-17, 2001.
[9] http://law.e-gov.go.jp/announce/H18HO098.html